植物单细胞转录组面临的挑战
一、植物单个细胞的分离
与动物细胞不同,植物细胞外被一层厚实且刚性的细胞壁包裹,这是植物单细胞转录组测序(scRNA‑seq)应用的关键限制因素。要获得高质量的转录本信息,必须先去除细胞壁制备原生质体,才能有效分离单个植物细胞,而细胞壁的存在极大制约了 scRNA‑seq 在植物研究中的广泛应用。
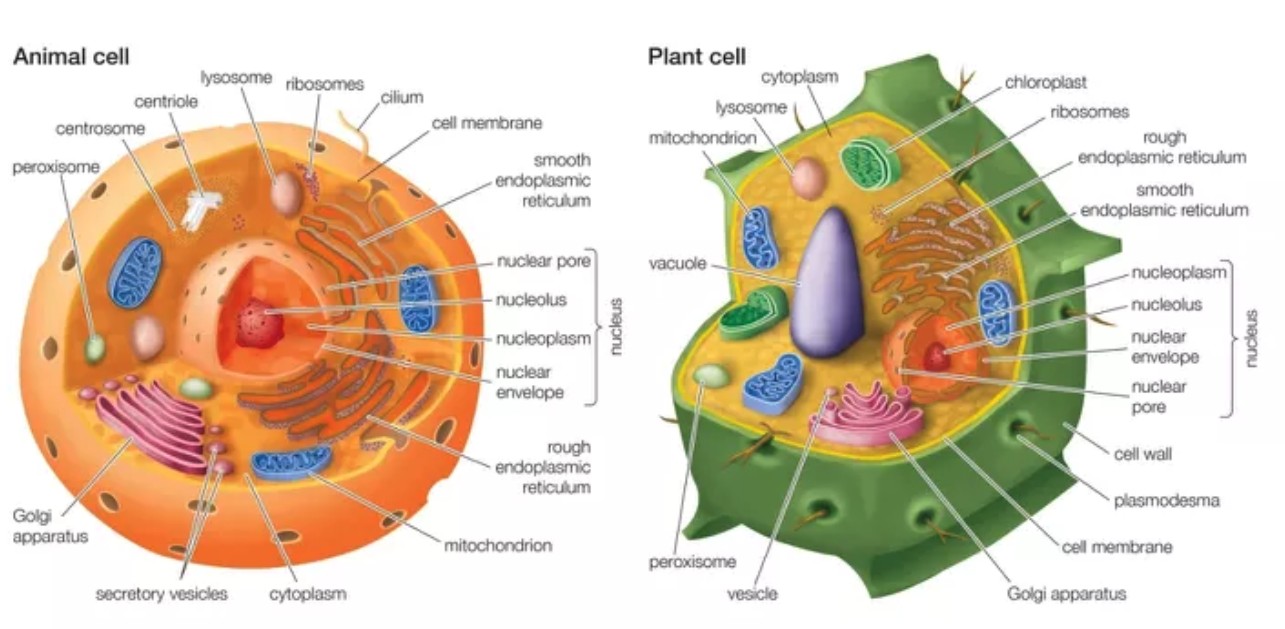
目前,原生质体制备法已应用于植物 scRNA‑seq 分析,但该技术体系仍高度依赖拟南芥、水稻等模式植物,主要得益于其成熟、稳定的原生质体提取流程。不同植物材料、不同细胞类型的细胞壁组分与结构差异显著,导致模式植物的标准化方案难以直接推广到多数非模式植物,无法稳定获得高质量原生质体。
在现有技术中,酶解法去壁制备原生质体仍是主流手段,但其分离效率受多重因素影响。部分细胞类型对酶解与解离过程具有天然抗性,难以被有效分离,使得测序结果偏向于易制备原生质体的细胞类型。同时,原生质体制备过程易诱发细胞产生异位基因表达,甚至造成部分细胞类型丰度下降或丢失,进而引入数据偏差,加剧细胞类型鉴定的偏倚。
近年来,研究者持续优化原生质体分离策略,植物原生质体制备困难的问题正逐步改善。与此同时,单核 RNA 测序(snRNA‑seq)逐渐成为植物 scRNA‑seq 的重要替代技术。该方法直接分离细胞核进行转录组测序,无需制备原生质体,显著拓展了植物单细胞研究的适用范围,尤其适用于难以酶解的新鲜组织以及固定或冻存样本。
snRNA‑seq 在很大程度上降低了传统 scRNA‑seq 的检测偏差,有效消除了细胞解离过程引发的转录应激响应。但已有研究显示,snRNA‑seq 对单个细胞核的基因捕获量相对有限。因此,该技术能否独立用于解析植物复杂组织的细胞类型异质性,仍需更多实验证据加以验证。
二、细胞大小的影响
植物细胞在体积上的高度异质性,为植物单细胞转录组测序分析带来了一系列技术难题,其中细胞大小是制约单细胞分离效率的核心因素。
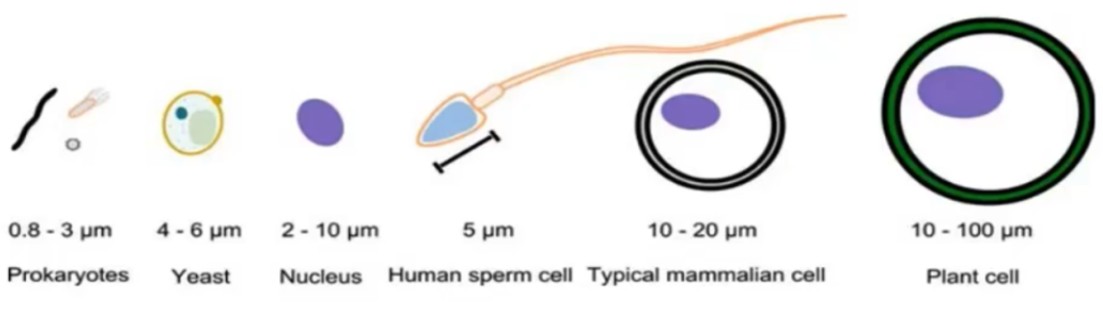
从细胞尺度对比,植物细胞体积远大于动物细胞:多数动物细胞直径集中在 10–30 μm,而成熟植物细胞直径最高可达 100 μm。这种显著的体积差异给高通量单细胞测序平台带来极大挑战。以目前应用最广泛的 10x Genomics 微流体测序平台为例,其微流控通道与油包水液滴系统存在严格的细胞尺寸限制,直径超过 40 μm 的植物细胞无法正常进入微流体通道,也难以完成稳定的包裹与标记。
这一技术局限会直接导致单细胞捕获出现明显的细胞类型偏好,大体积细胞被系统性排除,最终获得的 scRNA‑seq 数据无法真实反映植物组织内原始的细胞群体组成与转录组特征,造成实验结果与实际生物学状态的偏差。
针对细胞体积差异引发的分离偏好性问题,结合植物细胞结构特点,目前科研领域推荐采用不受细胞尺寸限制的研究方案:一方面可选用基于微孔阵列的单细胞分离系统,这类平台对细胞体积包容性更强,能适配不同大小的植物细胞;另一方面可优先采用单核 RNA 测序(snRNA‑seq),仅对分离得到的细胞核进行测序,绕开完整细胞的体积限制,从技术层面规避细胞大小带来的分离偏差,保障实验数据的真实性与全面性。
三、细胞类型的注释
细胞类型注释是植物 scRNA‑Seq 面临的另一项重要挑战。
随着 scRNA‑seq 在植物中的应用,目前已有三个植物单细胞转录组数据库为细胞分类提供了有力支撑:
- PCMDB 数据库(https://www.tobaccodb.org/pcmdb/homePage):包含拟南芥、玉米、水稻、大豆、番茄、烟草共 6 个植物物种的 Marker 基因,覆盖 263 种细胞类型,其中 3119 个标记基因经实验验证可靠。
- PsctH 数据库(http://jinlab.hzau.edu.cn/PsctH/):收集拟南芥、玉米、水稻、花生、番茄共 5 个物种的 Marker 基因,涉及 26 种细胞类型。
- PlantscRNAdb 数据库(http://ibi.zju.edu.cn/plantscrnadb/):包含拟南芥、水稻、番茄、玉米、草莓、杨树、烟草、浮萍、白菜、木薯、蒺藜苜蓿、裂叶荆芥、陆地棉、大豆、蝴蝶兰等 33 个物种的 Marker 基因。
总体来看,模式植物的细胞类型标记基因资源相对完善。但对于大多数非模式植物,可用的细胞类型标记基因仍然极少,无法准确确定细胞类型,进而难以开展后续分析。目前通常只能借助生物信息学方法,通过跨物种寻找同源基因来推定标记基因。
- 发表于 2026-03-30 09:17
- 阅读 ( 366 )
- 分类:转录组
你可能感兴趣的文章
- 玉米根单细胞转录组细胞类型注释代码 287 浏览
- 华大DNBC4单细胞转录组数据分析-拟南芥根愈伤组织单细胞转录组图谱 345 浏览
- scanpy 绘制marker基因点图 277 浏览
- 植物单细胞转录组文章 2298 浏览
- 拟南芥叶单细胞分析流程 1850 浏览
